Progressione dell’atrofia geografica
Le regioni di atrofia iniziano solitamente al di fuori della fovea e si espandono fino a coinvolgere la fovea, il che, nel tempo, porta alla perdita permanente della vista.1
Attualmente l’atrofia geografica colpisce oltre 5 milioni di persone in tutto il mondo. Si prevede che questo numero aumenterà a oltre 18 milioni entro il 2040.1
Dall’età di 50 anni la prevalenza
quadruplica ogni 10 anni.6
L’atrofia geografica rappresenta
fino al 20% di tutta la cecità legale attribuita alla DMLE.7,8
Un occhio affetto da atrofia geografica può inoltre sviluppare naturalmente la DMLE umida e viceversa.9
La percentuale di pazienti con DMLE umida progredita ad atrofia geografica nell’arco di una media di 7,3 anni di follow-up.10
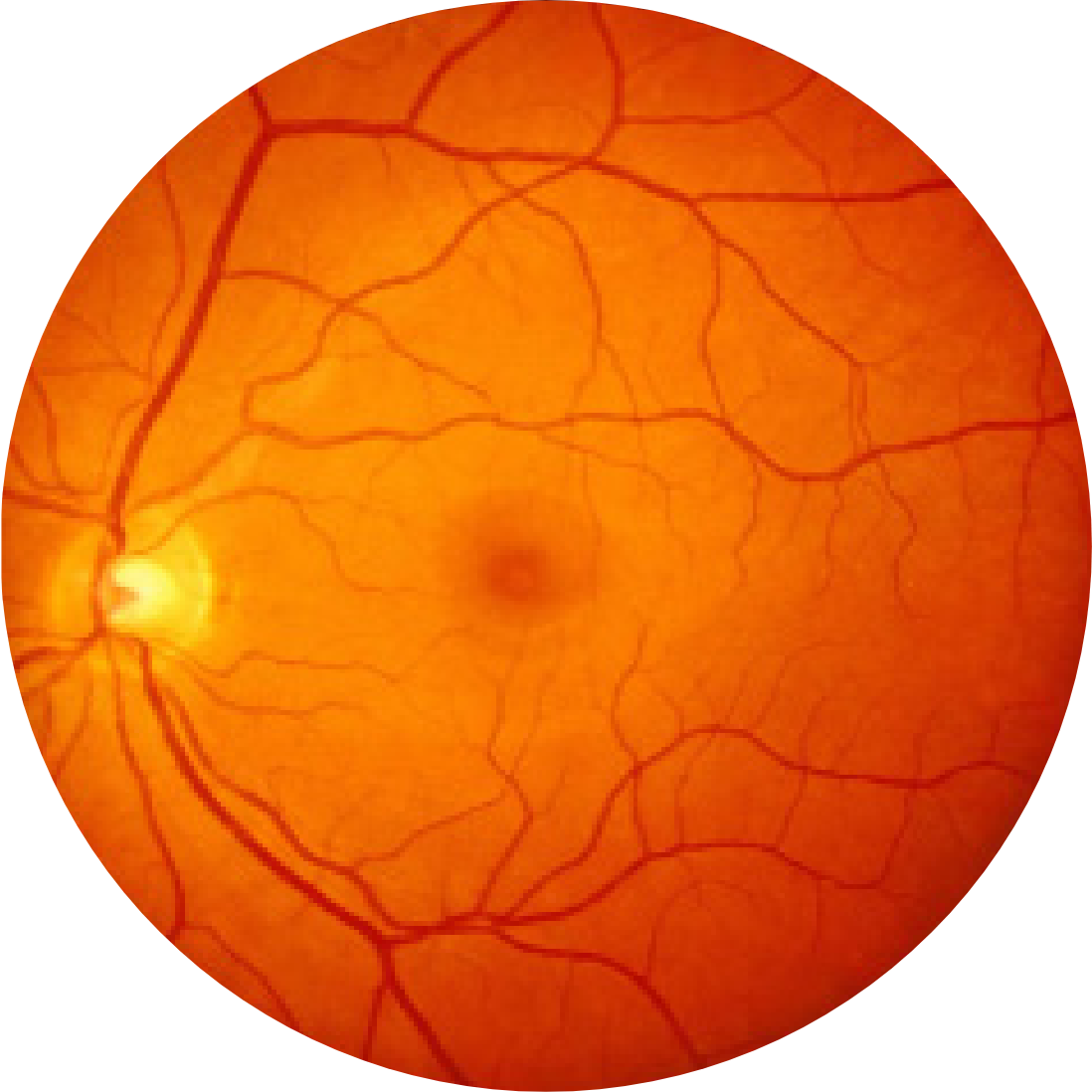
Fotografia del fondo oculare di un occhio sano
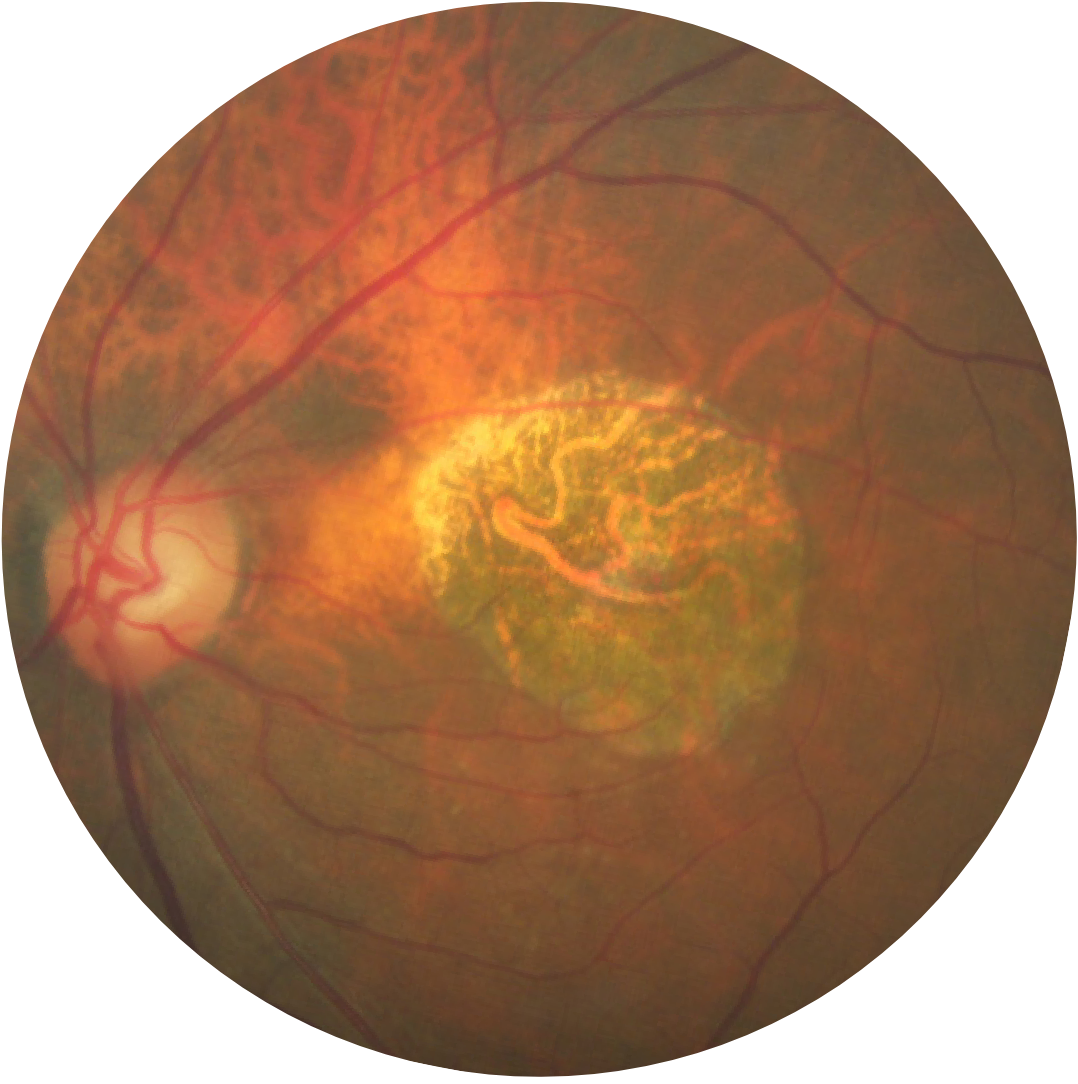
Fotografia del fondo oculare di un occhio con atrofia geografica
L’atrofia geografica è caratterizzata da una perdita progressiva e irreversibile dei fotorecettori, dell’epitelio pigmentato retinico (EPR) e della lamina coriocapillare sottostante.1,2
Le regioni di atrofia iniziano solitamente al di fuori della fovea e si espandono fino a coinvolgere la fovea, il che, nel tempo, porta alla perdita permanente della vista.1
Cause dell’atrofia geografica
La degenerazione maculare legata all’età è una malattia complessa, multifattoriale e la patogenesi dell’atrofia geografica coinvolge una complessa interazione di fattori genetici, fisiologici e ambientali.11-14
Genetica
- Formazione di drusen
- Formazione di specie reattive dell’ossigeno
- Infiammazione
- Risposta immunitaria, incluso il complemento
Fisiologia
- L’età è il fattore di rischio maggiore per l’atrofia geografica
- Alcuni tipi di dislipidemie
Ambiente
- Luce solare, fumo e dieta
- Elevato consumo di alcol
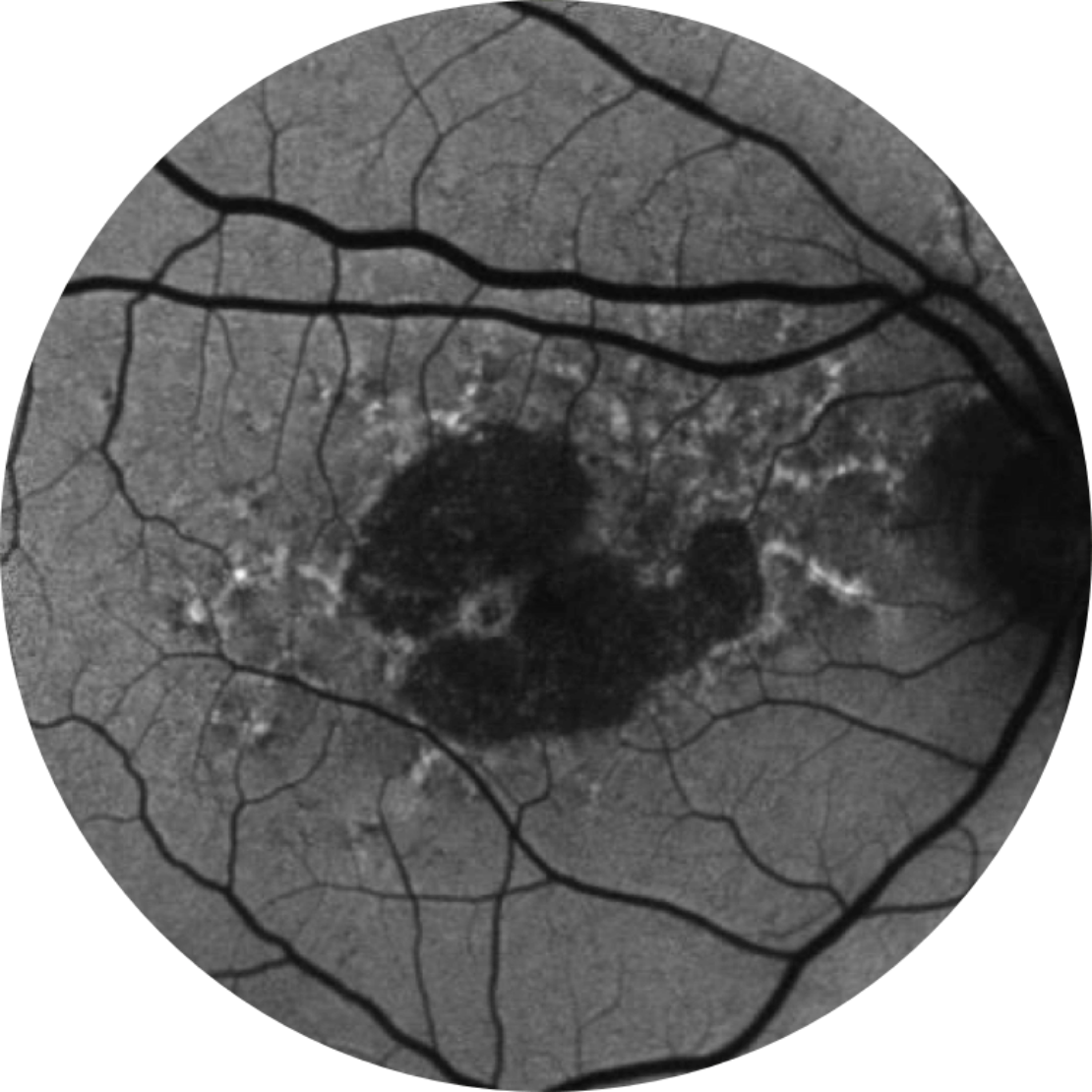
Basale Anno 1
BCVA 20/63+, area AG 5,18 mm2
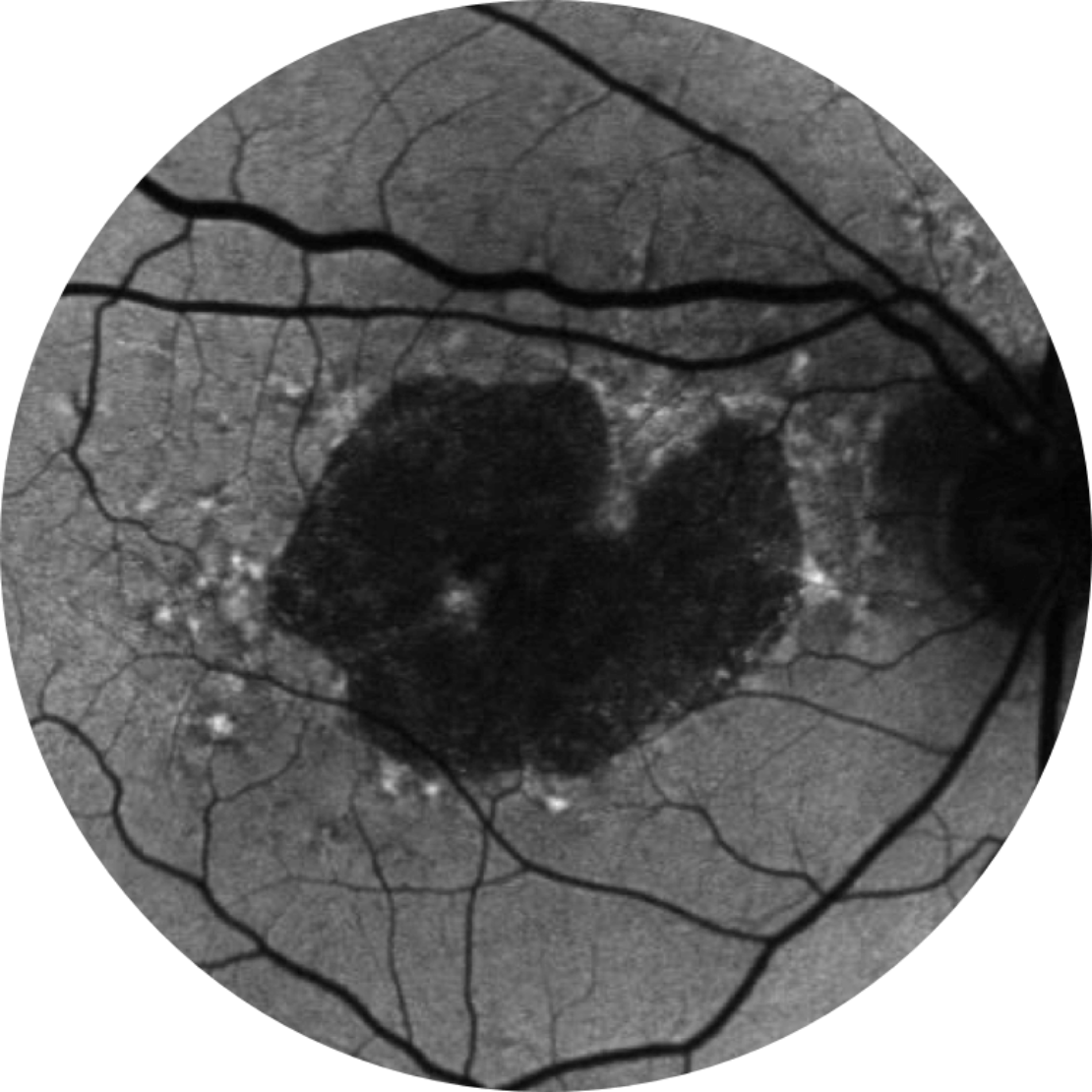
Basale Anno 2
BCVA 20/80-2, area AG 10,39 mm2
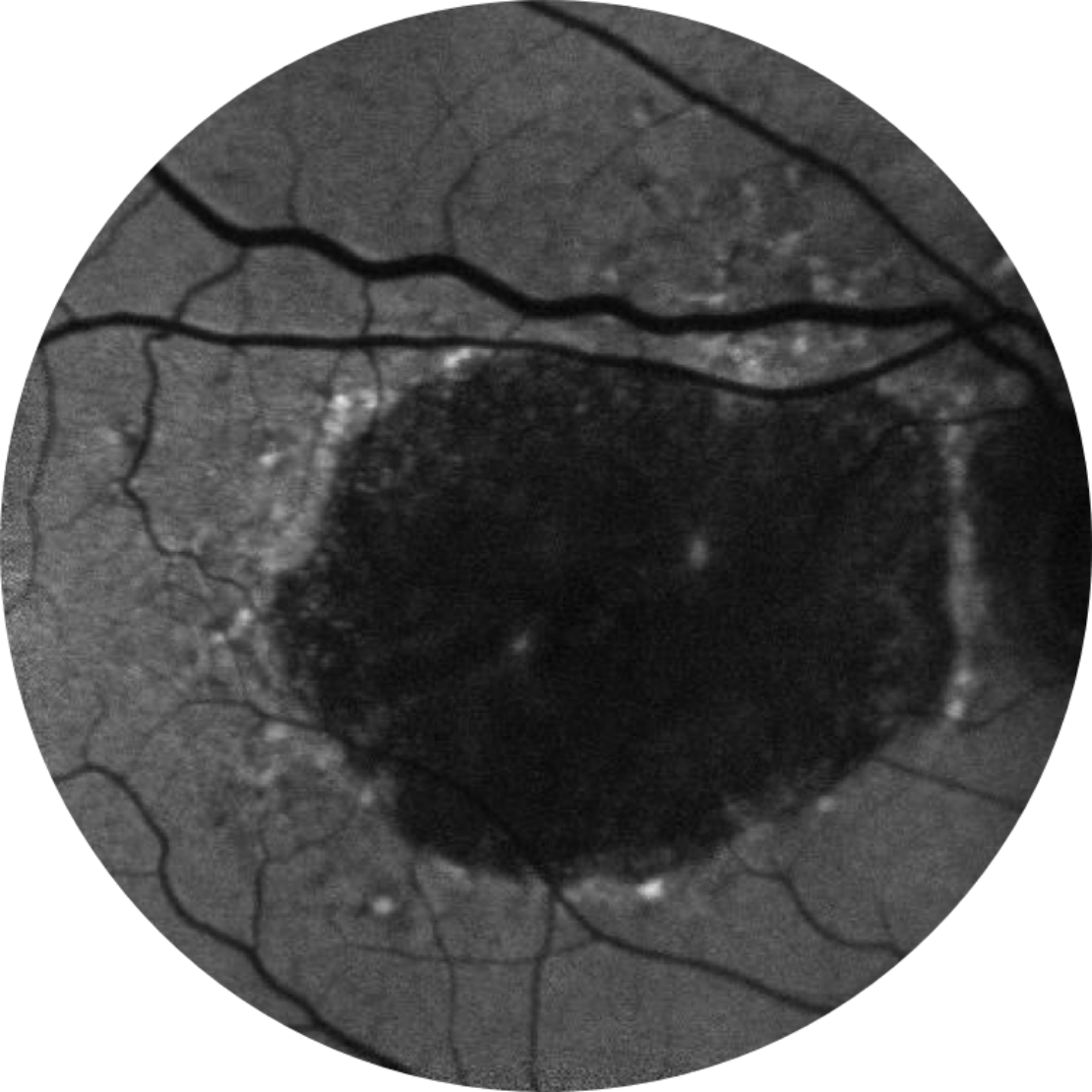
Basale Anno 5
BCVA 20/200, area AG 18,58 mm2
La crescita delle lesioni può portare a un declino della vista.2,16,17
L’acuità visiva non è fortemente correlata alla crescita delle lesioni dell’atrofia geografica. La visione funzionale diminuisce con la crescita delle lesioni.15
BCVA = Massima acuità visiva corretta (Best-Corrected Visual Acuity)
Diagnosi di atrofia geografica
Le tecniche di imaging retinico vengono utilizzate per identificare, diagnosticare e monitorare tutti gli stadi della degenerazione maculare legata all’età, inclusa l’atrofia geografica.18
Durante la diagnosi e il monitoraggio della degenerazione maculare legata all’età, un oftalmologo, uno specialista della retina o un optometrista valuteranno le seguenti caratteristiche nella retina:19
• Presenza di drusen
• Area nettamente demarcata nella regione maculare con retina atrofica, priva di pigmentazione
• Vasi sanguigni coroidali sottostanti visibili
Autofluorescenza normale del fondo oculare di una retina
L’angiografia con autofluorescenza del fondo oculare è attualmente una tecnologia di imaging standard per visualizzare l’epitelio pigmentato retinico (EPR) nell’atrofia geografica.20
Scansione OCT orizzontale sulla fovea
Tomografia a coerenza ottica (Optical Coherence Tomography, OCT): l’atrofia degli strati retinici può essere chiaramente osservata con questa tecnica di imaging non invasivo.21
Attuali approcci di gestione
Attenzione alla gestione della malattia, senza rallentare o arrestare la crescita delle lesioni.22-24

RIABILITAZIONE VISIVA25

AUSILI PER IPOVISIONE26

INTEGRATORI AREDS27
CESSAZIONE DEL FUMO27

ESERCIZIO28

DIETA27
AREDS = Studio sulle malattie oculari legate all’età (Age-Related Eye Disease Study).
Gli integratori AREDS non sono una terapia approvata per l’AG.
Approcci terapeutici attualmente in fase di studio
Ad oggi, non vi sono terapie approvate per ridurre il tasso di progressione della DMLE secca avanzata, sebbene diverse potenziali terapie siano in fase di studio.11

Scopri il ruolo dell’iperattivazione del complemento nell’atrofia geografica
Nella patogenesi dell’atrofia geografica potrebbero essere coinvolti vari pathway mediati dal complemento. L’inibizione del pathway del complemento è un bersaglio terapeutico interessante per rallentare la progressione dell’AG.29,30
Unisciti a noi nel nostro viaggio nell’atrofia geografica
Sii il primo a ricevere le ultime notizie sull’atrofia geografica
Grazie per aver inviato i tuoi dati.
Controlla le tue e-mail per verificare la tua iscrizione.
Bibliografia
- Fleckenstein, M. et al. (2018). The Progression of Geographic Atrophy Secondary to Age-Related Macular Degeneration. Ophthalmology, 125(3), 369–390. https://doi.org/10.1016/j.ophtha.2017.08.038.
- Boyer, D.S. et al. (2017). The pathophysiology of geographic atrophy secondary to age-related macular degeneration and the complement pathway as a therapeutic target. Retina, 37(5), pp.819–835. doi:10.1097/iae.0000000000001392.
- Lindblad, A.S. et al. (2009).Change in Area of Geographic Atrophy in the Age-Related Eye Disease Study. Archives of Ophthalmology, 127(9), p.1168. doi:10.1001/archophthalmol.2009.198.
- Holz, F.G. et al. (2014). Geographic atrophy: clinical features and potential therapeutic approaches. Ophthalmology, [online] 121(5), pp.1079–1091. doi:10.1016/j.ophtha.2013.11.023.
- Sunness, J.S et al. (2007). The long-term natural history of geographic atrophy from age-related macular degeneration: enlargement of atrophy and implications for interventional clinical trials. Ophthalmology, [online] 114(2), pp.271–277. doi:10.1016/j.ophtha.2006.09.016.
- Rudnicka, A.R. et al. (2012). Age and gender variations in age-related macular degeneration prevalence in populations of European ancestry: a meta-analysis. Ophthalmology, [online] 119(3), pp.571–580. doi:10.1016/j.ophtha.2011.09.027.
- Gehrs, K.M. et al. (2006). Age-related macular degeneration—emerging pathogenetic and therapeutic concepts. Annals of medicine, [online] 38(7), pp.450–471. doi:10.1080/07853890600946724.
- Biarnés, M. et al. (2011). Update on Geographic Atrophy in Age-Related Macular Degeneration. Optometry and Vision Science, 88(7), pp.881–889. doi:10.1097/opx.0b013e31821988c1.
- BrightFocus Foundation. (2018). Age-Related Macular Degeneration: Facts & Figures. [online] Disponibile all’indirizzo: https://www.brightfocus.org/macular/article/age-related-macular-facts-figures. Consultato il 29 aprile 2021.
- Rofagha, S. et al. (2013). Seven-Year Outcomes in Ranibizumab-Treated Patients in ANCHOR, MARINA, and HORIZON. Ophthalmology, 120(11), pp.2292–2299. doi:10.1016/j.ophtha.2013.03.046.
- Buschini, E. et al. (2015). Recent developments in the management of dry age-related macular degeneration. Clinical Ophthalmology, p.563. doi:10.2147/opth.s59724.
- Risk factors associated with age-related macular degeneration. (2000). Ophthalmology, 107(12), pp.2224–2232. doi:10.1016/s0161-6420(00)00409-7.
- Fritsche, L.G. et al. (2016). A large genome-wide association study of age-related macular degeneration highlights contributions of rare and common variants. Nature genetics, [online] 48(2), pp.134–143. doi:10.1038/ng.3448.
- Chong, E.W. et al. (2008). Alcohol Consumption and the Risk of Age-Related Macular Degeneration: A Systematic Review and Meta-Analysis. American Journal of Ophthalmology, [online] 145(4), pp.707-715.e2. doi:10.1016/j.ajo.2007.12.005.
- Heier, J.S. et al. (2020). Visual Function Decline Resulting from Geographic Atrophy: Results from the Chroma and Spectri Phase 3 Trials. Ophthalmology. Retina, [online] 4(7), pp.673–688. doi:10.1016/j.oret.2020.01.019.
- Kimel, M. et al. (2017). Functional Reading Independence (FRI) Index: A New Patient-Reported Outcome Measure for Patients With Geographic Atrophy. Investigative Opthalmology & Visual Science, 57(14), p.6298. doi:10.1167/iovs.16-20361.
- Sadda, S.R. Clinical endpoints for the study of geographic atrophy secondary to age-related macular degeneration. Retina, 36(10), pp.1806–1822. doi:10.1097/iae.0000000000001283.
- What is the difference between direct and indirect ophthalmoscopy (2016). What is the difference between direct and indirect ophthalmoscopy? [online] American Academy of Ophthalmology. Disponibile all’indirizzo: https://www.aao.org/eye-health/ask-ophthalmologist-q/what-is-difference-between-direct-indirect-ophthal. Consultato il 20 luglio 2022.
- eyewiki.aao.org. (n.d.). Geographic Atrophy – EyeWiki. [online] Disponibile all’indirizzo: https://eyewiki.aao.org/Geographic_Atrophy. Consultato il 20 luglio 2022.
- Townsend, W.D. (1992). Scleral depression. Optometry Clinics: The Official Publication of the Prentice Society, [online] 2(3), pp.127–144. Disponibile all’indirizzo: https://pubmed.ncbi.nlm.nih.gov/1463913.
- Ferguson, L.R. et al. (2014). Retinal Thickness Measurement Obtained with Spectral Domain Optical Coherence Tomography Assisted Optical Biopsy Accurately Correlates with Ex Vivo Histology. PLoS ONE, 9(10), p.e111203. doi:10.1371/journal.pone.0111203.
- Bandello, F. et al. (2017). Recent advances in the management of dry age-related macular degeneration: A review. F1000Research, 6, p.245. doi:10.12688/f1000research.10664.1.
- Chakravarthy, U. et al. (2018). Characterizing Disease Burden and Progression of Geographic Atrophy Secondary to Age-Related Macular Degeneration. Ophthalmology, 125(6), pp.842–849. doi:10.1016/j.ophtha.2017.11.036.
- Sacconi, R. et al. (2017). A Review of Current and Future Management of Geographic Atrophy. Ophthalmology and Therapy, [online] 6(1), pp.69–77. doi:10.1007/s40123-017-0086-6.
- Ramírez Estudillo, J.A. et al. (2017). Visual rehabilitation via microperimetry in patients with geographic atrophy: a pilot study. International Journal of Retina and Vitreous, [online] 3, p.21. doi:10.1186/s40942-017-0071-1.
- Gopalakrishnan, S. et al. (2020). Low-vision intervention in individuals with age-related macular degeneration. Indian Journal of Ophthalmology, [online] 68(5), pp.886–889. doi:10.4103/ijo.IJO_1093_19.
- Thorell, M.R. and Rosenfeld, P.J. (2014). Treatment of Geographic Atrophy: What’s on the Horizon? Current Ophthalmology Reports, 2(1), pp.20–25.
doi:10.1007/s40135-013-0036-y. - Seddon, J.M. (2003). Progression of Age-Related Macular Degeneration. Archives of Ophthalmology, 121(6), p.785. doi:10.1001/archopht.121.6.785.
- Katschke, K.J. et al. (2018). Classical and alternative complement activation on photoreceptor outer segments drives monocyte-dependent retinal atrophy. Scientific Reports, [online] 8(1), p.7348. doi:10.1038/s41598-018-25557-8.
- Heesterbeek, T.J. et al. (2020). Complement Activation Levels Are Related to Disease Stage in AMD. Investigative Ophthalmology & Visual Science, [online] 61(3), pp.18–18. doi:10.1167/iovs.61.3.18.
EU-GA-2200013